01出血与血栓:血管的“双面间谍”
对机体而言,血液脱离血管就是出血,血液滞留血管就是血栓。二者像一对孪生兄弟,在病理条件下此消彼长:组织受损→出血→启动止血→可能走向过度血栓。弄清这一连串事件,是诊断出血性疾病与血栓性疾病的核心。
02止血“三驾马车”
正常止血依赖三条平行却紧密相连的链条:完整的血管壁、足量的功能血小板、活性的凝血因子。任何一环掉链子,都可能让血液“想留留不住,想凝凝不住”。
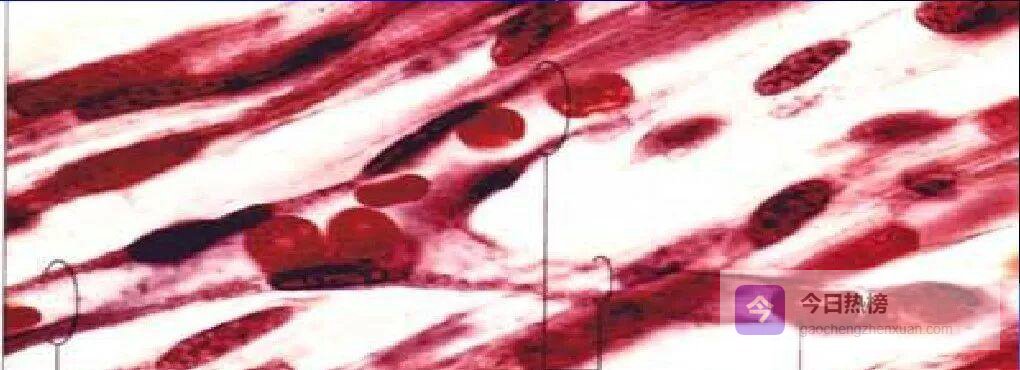 2.1 ❒ 血管壁:第一道“闸门”
2.1 ❒ 血管壁:第一道“闸门” 血管壁自内而外分为三层:
内皮层像一张紧密排列的单人床,合成并贮存 vWF、t-PA、TSP 等“信使蛋白”;
中膜层由胶原、平滑肌、弹力纤维构成,既撑起血管,也提供“血小板粘附码头”;
外膜层是血管与周围组织的“缓冲带”。
当血管受伤,内皮下的胶原暴露,就像打开了“报警开关”,后续所有止血步骤由此触发。
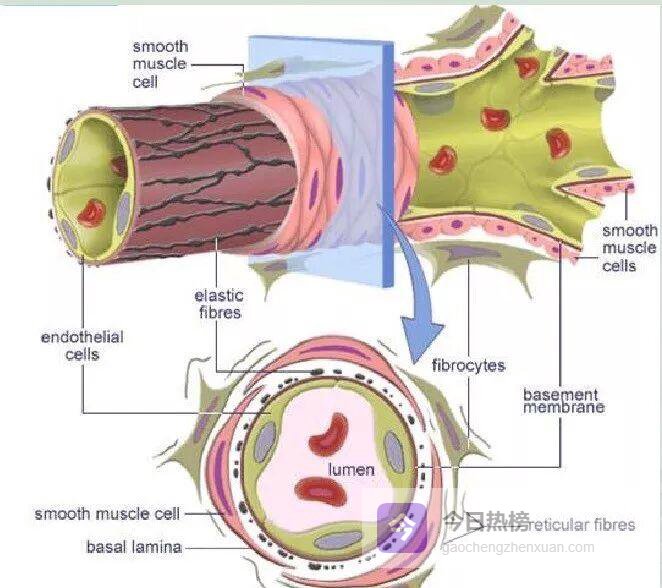 2.1.1 ❒ 血管收缩:伤口“第一扣”
2.1.1 ❒ 血管收缩:伤口“第一扣” 神经轴突反射与儿茶酚胺、TXA₂、5-HT 等递质共同让受损血管“捏紧拳头”,血流速度瞬间下降 50% 以上,为凝血物质堆积赢得时间。
2.1.2 ❒ 血小板“三步走”粘附:GPIb-Ⅸ 经 vWF 锚定在胶原上;
聚集:ADP、肾上腺素、凝血酶把血小板拧成“麻花”;
释放 & 促凝:颗粒内容物涌出,加速自身聚集并暴露 PF3,把“软伤口”变成“硬凝块”。
激肽释放与血小板释放的血管通透因子让血浆外渗、血液浓缩,局部血粘度可升高 3~4 倍,血流像酸奶一样缓慢,为后续纤维蛋白网打好地基。
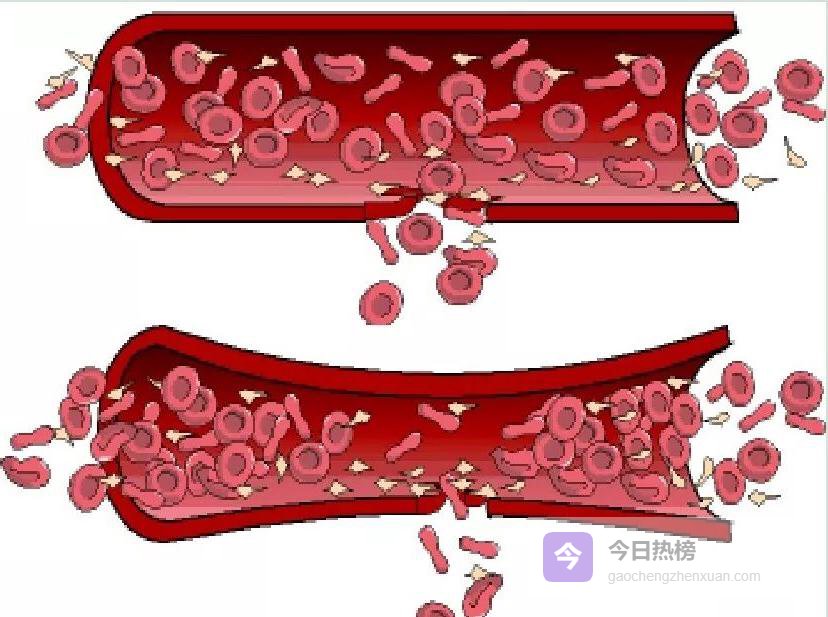 2.2 ❒ 血小板:超级“螺丝钉”
2.2 ❒ 血小板:超级“螺丝钉” 粘附——第一时间“贴”在损伤处;
聚集——把单个血小板拧成“绳”;
释放——把促凝因子、钙离子、腺苷酸等一次性甩进伤口;
收缩——把松软的纤维蛋白网压成硬块;
修复——填补脱落的内皮缺口,降低血管通透性,相当于给伤口贴上“创可贴”并打上“绷带”。
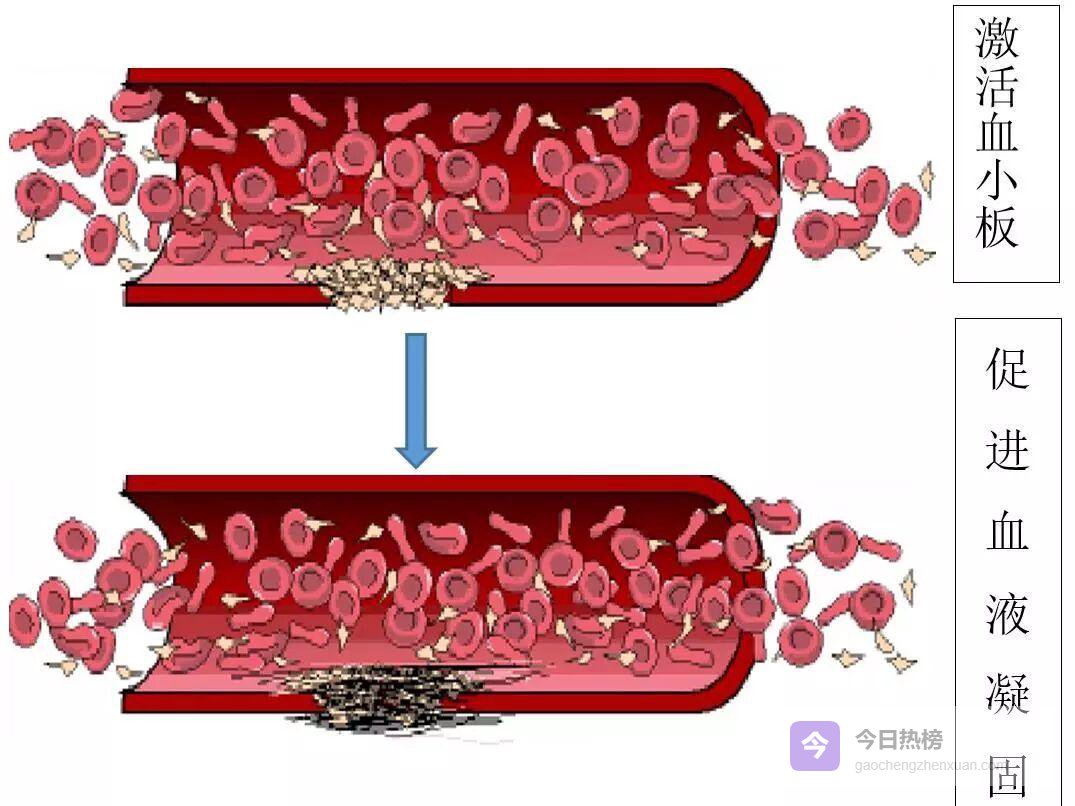
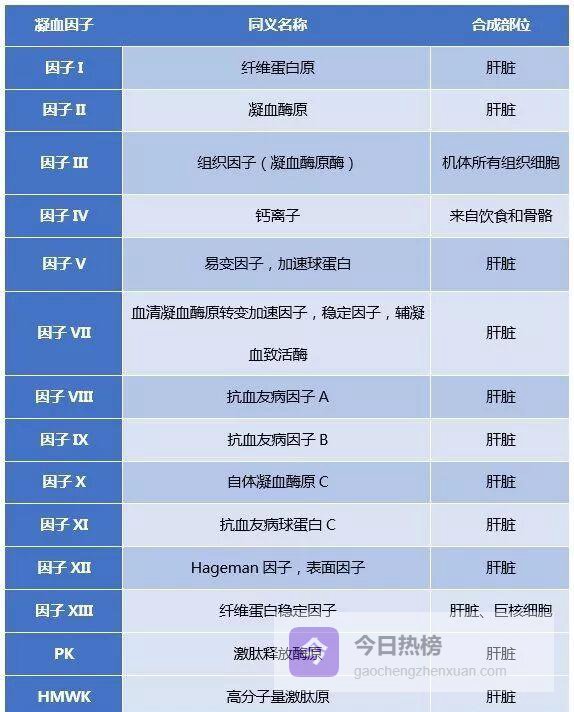
03凝血因子:14 张“王牌”如何分工
目前已确认的 14 个凝血因子各有性格:
依赖维生素 K 的四位“钙依赖型”(Ⅱ、Ⅶ、Ⅸ、Ⅹ)必须吃够维生素 K 才能“长出”γ-羧基谷氨残基;
接触因子三位“启动型”(Ⅺ、Ⅻ、HMWK/PK)靠“接触反应”点燃内源途径;
对凝血酶敏感的四位“快反应型”(Ⅰ、Ⅴ、Ⅷ、ⅩⅢ)一遇凝血酶就激活;
组织因子(Ⅲ)藏在细胞表面,一旦入血就与Ⅶ形成 1∶1 复合物,启动外源途径。
04凝血三阶段:从“启动”到“封口”
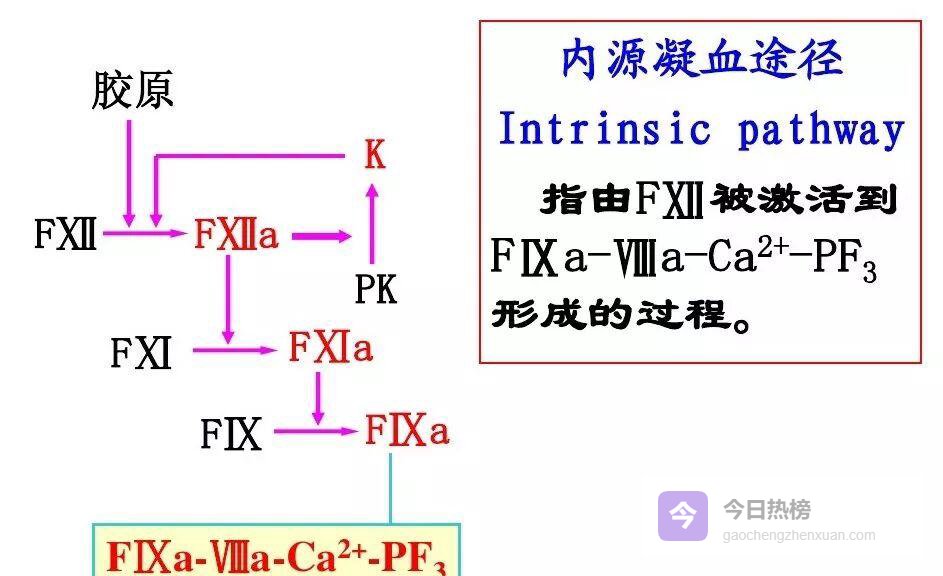
4.1 ❒ 内源性途径(12a→10a)带负电的损伤面激活Ⅻ→Ⅻa→Ⅺa→Ⅸa→Ⅹa,形成血浆凝血活酶,最终把纤维蛋白原变成纤维蛋白。临床用 APTT 当筛子,一测就知内源系统是否“掉线”。
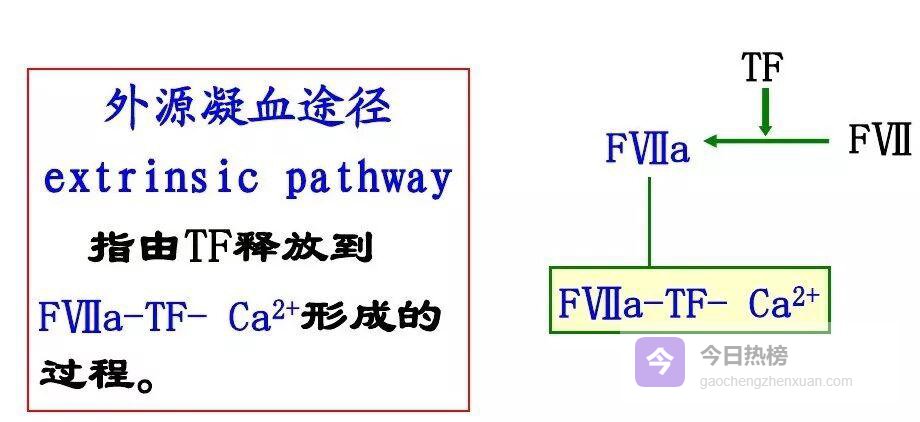
 4.2 ❒ 外源性途径(TF→7a→10a)
4.2 ❒ 外源性途径(TF→7a→10a) 组织损伤后 TF 入血,与Ⅶ形成复合物,无需接触相就能迅速激活Ⅹ。外源途径 快如闪电,但受 TFPI 这把“安全锁”严密调控。PT 是最常用的外源筛选试验。
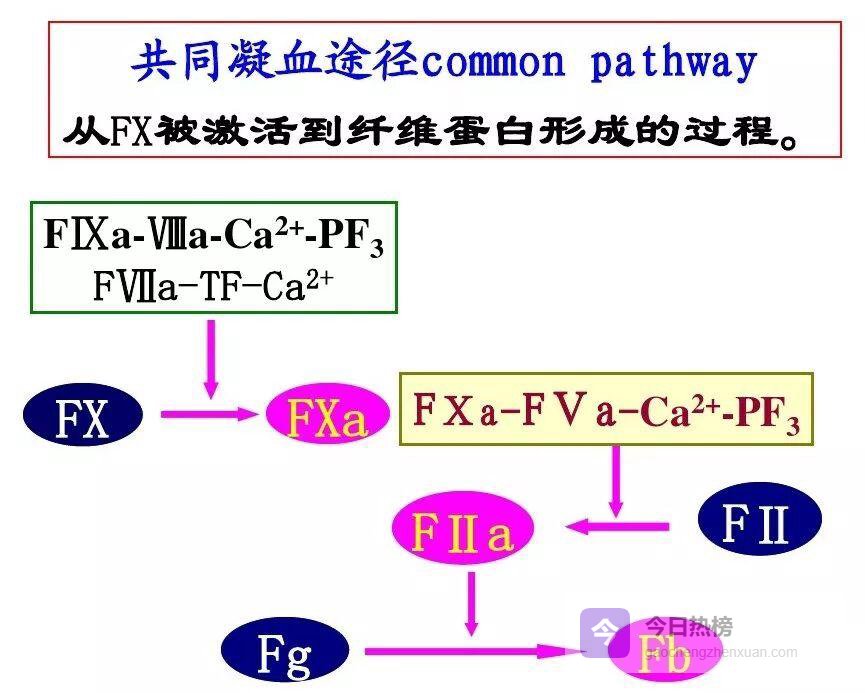
 4.3 ❒ 共同途径(10a→纤维蛋白)
4.3 ❒ 共同途径(10a→纤维蛋白) 一旦内外源交叉,Ⅹa 就把凝血酶原切成凝血酶,纤维蛋白原被水解成单体→聚合→交联,最终形成 不溶于尿素的稳定凝块。FPA/FPB 的释放量可反映凝血酶活性高低,成为高凝状态的新指标。纤维蛋白一旦生成,会像“海绵”一样吸附剩余凝血酶,防止其扩散。
05从实验室到临床:检验如何导航止血与血栓
常规项目如 血小板计数、凝血酶原时间、活化部分凝血活酶时间、D-二聚体、FDPs 等,可快速指向出血或血栓方向;若进一步做基因筛查、vWF 功能检测、FXIII活性测定,则能把罕见病如 Bernard-Soulier 综合征、AF3C 缺陷等揪出来。精准检测让医生在止血与溶栓之间走钢丝时,多了把安全尺。
原创文章,作者:胡佳慧,如若转载,请注明出处:http://m.gaochengzhenxuan.com/rebang/14067.html

